ほとんどの固体には、 結晶構造、その中で「構築」される粒子は特定の順序で並んでおり、それによって 結晶格子。 同一の構造単位の繰り返しから構築されます - 単位セル、隣接するセルと通信し、追加のノードを形成します。 その結果、14 種類の異なる結晶格子が存在します。
結晶格子の種類。
格子節点に立つ粒子に応じて、次のように区別されます。
- 金属結晶格子。
- イオン結晶格子。
- 分子結晶格子。
- 高分子(原子)結晶格子。
結晶格子内の金属結合。
イオン結晶は脆弱性が増大しています。 結晶格子の変化(たとえそれがわずかであっても)は、同じように荷電したイオンが互いに反発し始め、結合が切れ、亀裂や亀裂が形成されるという事実につながります。
結晶格子の分子結合。
分子間結合の主な特徴はその「弱さ」(ファンデルワールス、水素)です。

これが氷の構造です。 各水分子は水素結合によって周囲の 4 つの分子と結合し、四面体構造を形成します。
水素結合は、高沸点、融点、低密度を説明します。
結晶格子の高分子結合。
結晶格子の節には原子があります。 これらの結晶は次のように分けられます。 3種類:
- フレーム;
- 鎖;
- 層状構造。
フレーム構造ダイヤモンドは自然界で最も硬い物質の 1 つです。 炭素原子は 4 つの同一の共有結合を形成し、正四面体の形状を示します ( sp 3 - ハイブリダイゼーション)。 各原子には孤立電子対があり、隣接する原子と結合することもできます。 その結果、ノードには炭素原子のみが存在する三次元格子が形成されます。
このような構造を破壊するには多量のエネルギーが必要であり、そのような化合物の融点は高い(ダイヤモンドの場合、融点は 3500°C)。
層状構造各層内の共有結合の存在と層間の弱いファンデルワールス結合について話します。
例としてグラファイトを見てみましょう。 それぞれの炭素原子は sp 2 - ハイブリダイゼーション。 4 番目の不対電子は層間にファンデルワールス結合を形成します。 したがって、4 番目の層は非常に機動性があります。

結合が弱いため壊れやすく、鉛筆で観察できる「筆記性」 - 4番目の層が紙上に残ります。
グラファイトは優れた電流伝導体です (電子は層の平面に沿って移動できます)。
鎖構造酸化物を持っている(例えば、 それで 3 )、光沢のある針、ポリマー、一部の非晶質物質、ケイ酸塩(アスベスト)の形で結晶化します。
結晶格子
8年生
※教科書によると、 ガブリエルアン O.S.化学-8. M.: バスタード、2003 年。
目標。 教育的。固体の結晶状態と非晶質状態の概念を教えてください。 結晶格子の種類、化学結合の種類との関係、および結晶格子への影響について学びます。 物理的性質物質。
物質の組成の不変の法則について考えてみましょう。発達
。 論理的思考、観察スキル、結論を出す能力を養います。教育的
。 美的センスと集団主義を形成し、視野を広げるため。機器と試薬。
結晶格子のモデル、フィルムストリップ「組成と構造に対する物質の特性の依存性」、透明フィルム「化学結合。 物質の構造」; 粘土、チューインガム、樹脂、ワックス、食塩 NaCl、グラファイト、砂糖、水。勤務組織の形態。
グループ。方法とテクニック。
独立した仕事、デモンストレーションの経験、研究室での作業。
碑文。
レッスンの進行状況 教師。
結晶はいたるところで見つかります。 私たちはクリスタルの上を歩き、クリスタルで構築し、クリスタルからデバイスや製品を作り、テクノロジーと科学でクリスタルを広く使用し、クリスタルを食べ、クリスタルで癒し、生物の中にクリスタルを見つけ、デバイスの助けを借りて広大な宇宙道路に出ます。結晶でできている...
結晶とは何ですか?
あなたの目が原子や分子を見始めたところを少し想像してみてください。 成長が減少し、結晶に入ることができました。 私たちの授業の目的は、固体の結晶状態と非晶質状態とは何かを理解し、結晶格子の種類を知り、物質の組成の不変の法則を理解することです。
物質のどのような凝集状態が知られていますか?
ある王国、化学国家には塩素が存在していた。 そして、彼は古代のハロゲン族に属し、かなりの遺産を受け取っていましたが(彼は外部エネルギーレベルで7つの電子を持っていました)、非常に貪欲で嫉妬深く、怒りで黄緑色になったことさえありました。
彼は昼も夜もアルゴンのようになりたいという願望に悩まされていた。 彼は考えて考え、最終的に次のことを思いつきました。「アルゴンの外準位には 8 つの電子がありますが、私には 7 つしかありません。 だから、もう一つ電子を手に入れる必要がある、そうすれば私も高貴になるだろう。」 翌日、クロラスは秘蔵の電子を求めて旅に出る準備をしていましたが、遠くまで行く必要はありませんでした。家の近くで、サヤに入った豆が 2 つ入ったような、彼とよく似た原子に出会いました。
「聞いてください、兄弟、あなたの電子を私にください」とクロラスは言いました。
「いいえ、電子をくれたほうがいいです」と双子は答えました。
「分かった、それでは誰も怒らないように電子を結合させよう」と貪欲なクロリンは言い、後で電子を自分のものにすることを望んでいた。
レッスンの進行状況 しかし、そうではありませんでした。貪欲な塩素がそれらを味方に引き入れようとした必死の努力にもかかわらず、両方の原子は同じ電子を等しく共有していました。テーブル上の物質を見て、それらを 2 つのグループに分けます。 粘土、チューインガム、樹脂、ワックスは非晶質物質です。 多くの場合、一定の融点を持たず、流動性が観察され、規則正しい構造 (結晶格子) がありません。 逆に塩は 塩化ナトリウム、黒鉛と砂糖 –
結晶性物質 。 それらは、明確な融解温度、規則的な幾何学的形状、および対称性によって特徴付けられます。非晶質物質と結晶質物質の両方が使用されます。 結晶格子の種類とそれが物質の物理的特性に及ぼす影響について学びます。 準備したものは、化学結合の種類を繰り返すのに役立ちます。
クリエイティブなタスク
- おとぎ話。
極性の共有結合に関するおとぎ話
とある王国、『周期表』と呼ばれる国家に、一匹の小さな電子が住んでいました。 彼には友達がいなかった。 しかしある日、「エクスターナル・レベル」と呼ばれる村に、最初のものと全く同じ電子機器が彼の元にやって来た。 彼らはすぐに友達になり、いつも一緒に歩きましたが、どうしてペアになったのかさえ気づきませんでした。 これらの電子は共有結合と呼ばれます。
そこで友人たちはサークルに参加することに決めました。そこで彼らはこう言われました。このサークルに入るには、エネルギーレベルを完了する必要があります。 友人たちは腹を立ててとぼとぼと家に帰りました。 家では、エネルギーレベルを完了する方法を考えました。 すると突然Clがこう言いました。
- さあ、第 3 レベルから電子を 1 つください。
- つまり、どうやって与えるのですか? – ナが尋ねた。
- それで、それを受け取って私に渡してください。 あなたには 2 つのレベルがあり、すべて完了します。私には 3 つのレベルがあり、すべて完了します。 そうすれば私たちはサークルに受け入れられます。
「分かった、受け取って」ナはそう言って電子を手放した。
彼らがサークルに来ると、サークルのディレクターはこう尋ねました。「どうやってこんなことができたのですか?」 彼らは彼にすべてを話しました。 監督は「よくやった、みんな」と言い、彼らを自分の輪に迎え入れた。 監督はナトリウムに「+1」のカードを渡し、塩素には「-1」のカードを渡しました。
レッスンの進行状況 そして今、彼は金属も非金属も、すべての人をサークルに受け入れます。 そして、Na と Cl がしたのは、彼がイオン結合と呼んだものでした。 化学結合の種類についてよく理解していますか? この知識は結晶格子を研究するときに役立ちます。 物質の世界は広大で多様です。 彼らは最も多くのものを持っています異なるプロパティ 。 物理的なものと、化学的性質
物質。 どのような特性を物理的特性として分類しますか? 学生は次のように答えます。身体的状態
レッスンの進行状況 、色、密度、融点と沸点、水への溶解度、電気伝導度。物質の物理的特性を説明します。 O 2 、H 2 O、NaCl、黒鉛
と。
生徒は表に記入します。その結果、表は次の形式になります。
| テーブル 物理的な |
プロパティ | |||
|---|---|---|---|---|
| 物質 | O2 | H2O | 塩化ナトリウム | |
| C | 物理的状態 | ガス | 液体 | 液体 |
| 固体 | 密度、g/cm 3 | 1,000 | 2,165 | 2,265 |
| 1.429 (g/l) | 色 | 色 | 無色 | 白 |
| 黒 t | –218,8 | 0,0 | +801,0 | – |
| 黒プリ、°С | –182,97 | +100 | +1465 | +3700 |
| キップ、°С | 水への溶解度 | – | わずかに溶ける | 解散しましょう |
| 不溶性 | 電気伝導率 | 非導電性 | 弱い | 弱い |
レッスンの進行状況 導体
物質の物理的特性に基づいて、その構造を決定できます。
レッスンの進行状況透明性。結晶は、その粒子 (原子、分子、イオン) が特定の周期的に繰り返される順序 (節点) で配置されている固体です。 精神的にノードを線で接続すると、空間的な枠組み、つまり結晶格子が形成されます。 結晶格子には 4 つのタイプがあります (スキーム 2) ).
、p. を参照してください。 24
スキーム 2
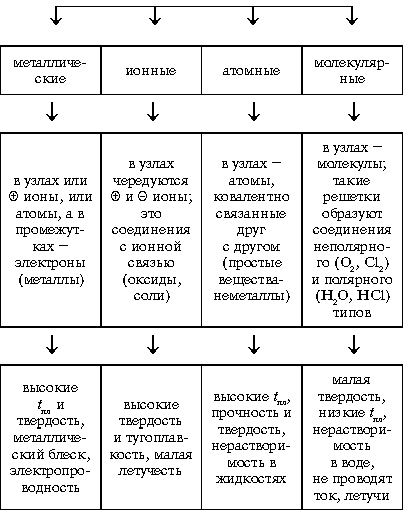
レッスンの進行状況 結晶格子結晶格子の働き ?
O 2、H 2 O、NaCl、C生徒たちの答え。
O 2 と H 2 O は分子結晶格子であり、NaCl はイオン格子です。
C – 原子格子。
結晶格子モデルのデモンストレーション:
レッスンの進行状況NaCl、C(グラファイト)、Mg、CO2。 結晶格子の種類に注目周期表内の位置に応じて異なります(教科書の79ページ)。
単体では見られない格子の種類は何ですか?
O 2、H 2 O、NaCl、C単体物質にはイオン格子がありません。
 |
|
レッスンの進行状況 分子格子を持つ物質は、昇華または昇華という現象によって特徴付けられます。
デモンストレーション体験。
安息香酸またはナフタレンの昇華。 (昇華とは、固体が (加熱されたときに) 液相を迂回して気体に変化し、その後再び霜の形で結晶化することです。)
レッスンの進行状況分子構造を持つ物質は、その物質の組成の不変の法則に従います。 分子構造の物質は、その調製方法に関係なく、一定の組成を持っています。 この法則はJ.L.プルーストによって発見されました。 彼はK.L.バーソレットとJ.ダルトンの間の長い論争を前者を支持して解決した。
たとえば、二酸化炭素または一酸化炭素 (IV) CO2 - 分子構造の複雑な物質。 炭素と酸素の 2 つの元素で構成されており、分子には 1 つの炭素原子と 2 つの酸素原子が含まれています。 相対分子量 M r ( CO2 ) = 44、モル質量 M( CO2 ) = 44 g/mol。 CO2 モル体積 V M ( CO2 ) = 22.4 モル (n.s.)。
物質 1 モル中の分子の数 N A (
) = 6 10 23 分子。
イオン構造を持つ物質の場合、プルーストの法則は必ずしも満たされません。
グラフィックディクテーション
「化学結合の種類と結晶格子の種類」
記号「+」と「-」は、このステートメント (1 ~ 20) が指定されたオプションの化学結合のタイプに典型的であるかどうかを示します。
オプション 1。
イオン結合。
オプション 2。
非極性の共有結合。
オプション 3。
極性の共有結合。
声明。
1. 金属原子と非金属原子の間に結合が形成されます。
2. 金属原子間に結合が形成されます。
3. 非金属原子間に結合が形成されます。
4. 原子の相互作用中にイオンが形成されます。
5. 結果として得られる分子は分極しています。
6. 結合は、共有電子対を移動させずに電子を対にすることによって確立されます。 7. 結合は、電子をペアにし、共通のペアを原子の 1 つに移動することによって確立されます。 8.進行中 化学反応起こっている
フルトランスミッション
反応する元素のある原子から別の原子への価電子。
9. 分子内の原子の酸化状態はゼロです。
10. 分子内の原子の酸化状態は、授受される電子の数に等しい。
13. このタイプの化学結合を持つ化合物は、分子タイプの結晶格子によって特徴付けられます。
14. このタイプの結合を持つ化合物は原子結晶格子を形成します。
15. 化合物は次の場合にガス状になることがあります。 通常の状態.
16. 化合物は通常の状態では固体です。
17. このタイプの接続は通常、難治性です。
18. このタイプの結合を持つ物質は、通常の条件下では液体である可能性があります。
19. このような化学結合を持った物質には臭いがつきます。
20. このような化学結合を持つ物質は金属光沢を持ちます。
答え(自尊心)。
オプション 1
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| + | – | – | + | + | – | – | + | – | + |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| – | + | – | – | – | + | + | – | – | – |
オプション 2
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| – | – | + | – | – | + | – | – | + | – |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| – | – | + | – | + | + | – | + | + | – |
オプション 3
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| – | – | + | – | + | – | + | – | – | – |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| + | – | + | + | + | – | + | + | + | – |
評価基準:1~2 エラー「5」、3~4 エラー「4」、5~6 エラー「3」。
素材を固定する
シリコンには原子結晶格子があります。 その物理的特性は何ですか?
Na 2 SO 4 はどのような結晶格子を持っていますか?
CO 2 酸化物は低い 黒 pl、および石英 SiO 2 – 非常に高い (石英は 1725 °C で溶けます)。 どのような結晶格子を持つべきでしょうか?
レッスンの進行状況 物事の本質を調べましたね。 結論として、ダイヤモンド、サファイア、エメラルド、アレキサンドライト、アメジスト、真珠、オパールなどの宝石について触れたいと思います。宝石には治癒効果があると長い間考えられてきました。 アメジストの結晶は酔いを防ぎ、幸せな夢をもたらすと信じられていました。 エメラルドは嵐から救います。 ダイヤモンドは病気から守ってくれます。 11月にはトパーズが、1月にはガーネットが幸福をもたらします。
宝石は王子や皇帝の富の尺度として機能しました。 17世紀に訪れた外国大使。 ロシアでは、彼らは自分たちが「 静かな恐怖「豪華な衣装を見て、 王室、完全に宝石がちりばめられています。
イリーナ・ゴドゥノワ皇后の頭には、「胸壁のある壁のような」王冠があり、ルビー、トパーズ、ダイヤモンド、「ランプパール」で巧みに作られた12の塔に分かれており、王冠の周りには巨大なアメジストとサファイアが散りばめられていました。 。
 |
タウリデのポチョムキン王子の帽子にはダイヤモンドがちりばめられており、そのために非常に重かったため、所有者は頭にかぶることができなかったことが知られています。 副官は帽子を手に持って王子の後ろに運んだ。 エリザベス皇后のドレスの1つは、あまりにも多くの宝石で縫い付けられていたため、彼女はその重みに耐えられず、舞踏会で気を失った。 しかし、さらに以前に、皇帝アレクサンドル・ミハイロヴィチの妻にもっと迷惑な事件が起こった。彼女は宝石が散りばめられた衣装を脱ぐために結婚式を中断しなければならなかったのだ。
世界最大のダイヤモンドは、それぞれ「オルロフ」、「シャー」、「コンクール」、「リージェント」などの独自の名前で知られています。
水晶は時計、音響測深機、マイクなどに必要です。 ダイヤモンド – 「労働者」(ベアリング、ガラスカッターなど)。
「現在人間の手に渡っている石は、楽しいものや贅沢なものではありませんが、私たちがその地位を取り戻すことができた素晴らしい素材であり、より美しく、より楽しく生きることができる素材です。 彼はそうしないよ」 宝石” – その時は過ぎました。それは人生に美しさを与える宝石となるでしょう。 ...彼の中に、人は自然そのものの比類のない色彩と不朽性の具体化を見るでしょう、芸術家はインスピレーションの燃える火によってのみ触れることができます」と学者A.E.フェルスマンは書いています。
水晶は自宅でも育てることができます。 創造的なクリスタル成長の宿題に挑戦してください。
宿題
「成長するクリスタル」
。 美的センスと集団主義を形成し、視野を広げるため。グラス、ボール紙、鉛筆、糸をきれいにします。 水、塩 (NaCl、CuSO 4、または KNO 3)
作業の進捗状況
最初の方法.
選択した塩の飽和溶液を準備します。 この目的のために、 お湯塩を少しずつ加え、溶けるまでかき混ぜます。 塩の溶解が止まるとすぐに、溶液は飽和します。
溶液をガーゼで濾過します。 この溶液をグラスに注ぎ、糸と重り(ボタンなど)の付いた鉛筆を置きます。 2 ~ 3 日後には、貨物が結晶で覆われているはずです。.
第二の方法
飽和溶液の入った瓶を厚紙で覆い、ゆっくりと冷却しながら結晶が底に落ちるまで待ちます。 ナプキンの上で結晶を乾燥させ、最も魅力的な結晶をいくつか糸で留め、鉛筆に結び付けて、他の結晶を除いた飽和溶液に入れます。 結晶が成長するまでに 2 ~ 3 週間かかる場合があります。 固体は通常、結晶構造を持っています。 これは、空間内の厳密に定義された点に粒子が正しく配置されることが特徴です。 これらの点が直線の交差によって精神的に接続されると、空間フレームが形成されます。結晶格子 。 粒子が存在する点は次のように呼ばれます。結晶格子ノード 。 仮想格子のノードには、イオン、原子、または分子が含まれる場合があります。 彼らは振動的な動きをします。 温度が上昇すると、振動の振幅が増加し、次のようになります。熱膨張
電話番号
粒子の種類と粒子間の結合の性質に応じて、イオン (NaCl、KCl)、原子、分子、金属の 4 種類の結晶格子が区別されます。 イオンからなる結晶格子をこう呼びます。。 それらはイオン結合を持つ物質によって形成されます。 例としては、各ナトリウム イオンが 6 つの塩化物イオンに囲まれ、各塩化物イオンが 6 つのナトリウム イオンに囲まれている塩化ナトリウムの結晶があります。
NaCl結晶格子
結晶または個々の分子内の特定の粒子に密接に隣接する最近接粒子の数は、と呼ばれます。 焦点番号.
NaCl 格子では、両方のイオンの配位数は 6 に等しいため、NaCl 結晶では個々の塩分子を分離することは不可能です。 何もありません。 結晶全体は、以下から構成される巨大な高分子と見なされるべきです。 等しい数イオン Na + および Cl -、Na n Cl n – ここで、n は大きな数です。 このような結晶内のイオン間の結合は非常に強いです。 したがって、イオン格子を持つ物質は比較的高い硬度を持ちます。 それらは耐火性があり、低空飛行します。
イオン結晶の融解は、イオンの相互に対する幾何学的に正確な配向を破壊し、それらの間の結合の強度を低下させます。 したがって、それらの溶融物は電流を伝導します。 イオン性化合物は一般に、水などの極性分子からなる液体に容易に溶解します。
ノードに個々の原子を含む結晶格子は、と呼ばれます。 原子。 このような格子内の原子は、強い共有結合によって互いに接続されています。 例としては、炭素の修飾の 1 つであるダイヤモンドが挙げられます。 ダイヤモンドは炭素原子で構成されており、各炭素原子は隣接する 4 つの原子と結合しています。 ダイヤモンドの炭素の配位数は 4 です。原子の結晶格子を持つ物質は融点が高く (ダイヤモンドは 3500 ℃以上)、強くて硬く、水にはほとんど溶けません。
分子(極性および非極性)から構成される結晶格子は、と呼ばれます。 分子。 このような格子内の分子は、比較的弱い分子間力によって互いに結合されています。 したがって、分子格子を有する物質は硬度が低く、融点が低く、水に不溶または難溶であり、その溶液はほとんど電流を通さない。 それらの例としては、氷、固体 CO 2 (「ドライアイス」)、ハロゲン、水素の結晶、酸素、窒素、希ガスなどが挙げられます。
価数
得られる分子内の相互作用する原子の数を示す重要な定量的特性は、 価数– ある元素の原子が他の元素の特定の数の原子を結合する性質。
原子価は、特定の元素が追加または置換できる水素原子の数によって定量的に決定されます。 たとえば、フッ化水素酸 (HF) ではフッ素は 1 価、アンモニア (NH 3) では窒素は 3 価、水素シリコン (SiH 4 - シラン) ではシリコンは 4 価などです。
その後、原子の構造に関する考え方の発展に伴い、元素の価数は不対電子の数(価数)と関連付けられるようになり、そのおかげで原子間の結合が行われます。 したがって、価数は、(基底状態または励起状態で) 化学結合の形成に関与する原子内の不対電子の数によって決まります。 一般に、価数は、特定の原子を他の元素の原子と接続する電子対の数に等しくなります。
イオン性化合物 (たとえば、塩化ナトリウム NaCl) は、そのイオンの電荷 (「+」と「-」) の間に強力な静電引力が存在するため、硬くて耐火性があります。
マイナスに帯電した塩素イオンは、「その」Na+ イオンだけでなく、その周囲の他のナトリウムイオンも引き付けます。 これは、どのイオンの近くにも、反対の符号を持つイオンが 1 つではなく、複数存在するという事実につながります (図 1)。
米。 1
実際、各塩素イオンの周囲には 6 つのナトリウムイオンがあり、各ナトリウムイオンの周囲には 6 つの塩素イオンがあります。
この規則正しいイオンの充填はイオン結晶と呼ばれます。 結晶内で単一の塩素原子が孤立している場合、その周囲のナトリウム原子の中から、塩素が反応したナトリウム原子を見つけることはもはや不可能です。 イオンは静電力によって互いに引き付けられるため、外力や温度上昇の影響を受けてもその位置を変えることを非常に嫌がります。 しかし、温度が非常に高い場合 (約 1500°C)、NaCl が蒸発し、二原子分子が形成されます。 これは、共有結合力が完全にオフになることはないことを示唆しています。
イオン結晶は、融解温度が高く、通常は大きなバンドギャップを持ち、高温でのイオン伝導性と多くの特定の光学特性 (スペクトルの近赤外領域での透明性など) を備えていることが特徴です。 単原子イオンと多原子イオンの両方から構築できます。 最初のタイプのイオン結晶の例は、アルカリ金属およびアルカリ土類金属のハロゲン化物の結晶です。 陰イオンは球状の密充填または球状の密な積み重ねの法則に従って配置され、陽イオンは対応する空隙を占めます。 ほとんど 特徴的な構造このタイプは、NaCl、CsCl、CaF2 です。2 番目のタイプのイオン結晶は、同じ金属の単原子陽イオンと有限または無限の陰イオン フラグメントから構築されます。 末端アニオン (酸性残基) - NO3-、SO42-、СО32- など。酸性残基は、無限の鎖や層に接続されたり、空洞内にカチオンが位置する三次元フレームワークを形成したりできます。たとえば、ケイ酸塩の結晶構造における。 イオン結晶の場合、結晶構造 U (表を参照) のエネルギーを計算できます。これは昇華のエンタルピーにほぼ等しくなります。 結果は実験データとよく一致しています。 Born-Mayer 方程式によれば、形式的には 1 価のイオンで構成される結晶の場合、次のようになります。
U = -A/R + Be-R/r - C/R6 - D/R8 + E0
- (R は最短のイオン間距離、A は構造の幾何学的形状に応じたマーデルング定数、B と r は粒子間の反発を表すパラメーター、C/R6 と D/R8 は対応する双極子間および双極子間四極子を特徴づけますイオンの相互作用、E
- 0 - ゼロ点エネルギー、e
- - 電子電荷)。 カチオンが大きくなるにつれて、双極子相互作用の寄与が増加します。
食卓塩は、食品添加物や食品保存料として使用される塩化ナトリウムです。 にも使用されます 化学工業、 薬。 か性ソーダやソーダなどを製造するための最も重要な原料として使われています。 食塩の式はNaClです。
ナトリウムと塩素の間のイオン結合の形成
塩化ナトリウムの化学組成は、ナトリウム原子と塩素原子の数が等しいという考えを与える従来の式 NaCl に反映されています。 しかし、物質は二原子分子によって形成されているのではなく、結晶で構成されています。 アルカリ金属が強力な非金属と反応すると、各ナトリウム原子はより電気陰性度の高い塩素を放出します。 ナトリウム陽イオンNa + と酸残基の陰イオンが出現 塩酸 Cl - 。 逆に荷電した粒子が互いに引き合い、イオン結晶格子を持つ物質を形成します。 小さなナトリウムカチオンは、大きな塩素アニオンの間に位置します。 塩化ナトリウムの組成中のプラスの粒子の数はマイナスの粒子の数に等しく、物質全体は中性です。
化学式。 食卓塩と岩塩
塩はイオン構造の複雑な物質であり、その名前は酸性残基の名前で始まります。 食塩の式はNaClです。 地質学者はこの組成の鉱物を「岩塩」と呼びます。 堆積岩-「岩塩」。 時代遅れ 化学用語製造時によく使われるのが「塩化ナトリウム」です。 この物質は以下の症状を持つ人々に知られています。 古代、かつては「白い金」と考えられていました。 現代の学童や学生は、塩化ナトリウムを含む反応式を読むときに化学記号 (「塩素ナトリウム」) を使用します。
物質の公式を使用して簡単な計算を実行してみましょう。
1) Mr (NaCl) = Ar (Na) + Ar (Cl) = 22.99 + 35.45 = 58.44。
相対値は 58.44 (amu) です。
2) モル質量は数値的には分子量に等しいですが、この量の測定単位は g/mol です: M (NaCl) = 58.44 g/mol。
3) 100 g の塩サンプルには、60.663 g の塩素原子と 39.337 g のナトリウムが含まれています。
食塩の物性
脆い岩塩の結晶は無色または白色です。 自然界には、灰色、黄色、青色の岩塩の堆積物もあります。 鉱物物質が赤みを帯びることがありますが、これは不純物の種類と量が原因です。 岩塩の硬度はわずか2〜2.5で、ガラスの表面には線が残ります。

塩化ナトリウムのその他の物理パラメータ:
- 匂い - 存在しない。
- 味 - 塩味。
- 密度 - 2.165 g/cm3 (20 °C);
- 融点 - 801 °C;
- 沸点 - 1413 °C;
- 水への溶解度 - 359 g/l (25 °C)。
研究室での塩化ナトリウムの調製
金属ナトリウムが試験管内で塩素ガスと反応すると物質が生成される 白- 塩化ナトリウム NaCl (食塩配合)。

化学は以下の洞察を提供します さまざまな方法で同じ接続を取得します。 以下にいくつかの例を示します。
NaOH (水溶液) + HCl = NaCl + H2O。
金属と酸の間の酸化還元反応:
2Na + 2HCl = 2NaCl + H2。
金属酸化物に対する酸の影響: Na 2 O + 2HCl (水溶液) = 2NaCl + H 2 O
弱酸をその塩の溶液からより強いものに置き換える:
Na 2 CO 3 + 2HCl (水溶液) = 2NaCl + H 2 O + CO 2 (ガス)。
これらの方法はすべて、工業規模で使用するには高価かつ複雑すぎます。
食塩の製造
文明の黎明期でさえ、人々は肉や魚を塩漬けにした方が長持ちすることを知っていました。 透明で規則的な形をした岩塩の結晶は、一部の古代の国でお金の代わりに使用され、その重さは金の価値がありました。 岩塩鉱床の探索と開発により、人口と産業の増大するニーズを満たすことが可能になりました。 食塩の最も重要な天然源:
- さまざまな国の岩塩鉱物の鉱床。
- 海、海、塩湖の水。
- 塩辛い貯水池のほとりにある岩塩の層と地殻。
- 火山の火口の壁にある岩塩の結晶。
- 塩性湿地。

業界では、食卓塩を製造するために 4 つの主な方法が使用されています。
- 地下層からの岩塩の浸出、得られた塩水の蒸発。
- での採掘;
- 塩湖の蒸発または塩水(乾燥残留物の質量の77%は塩化ナトリウム)。
- 塩水脱塩の副産物を使用します。
塩化ナトリウムの化学的性質

組成に関して言えば、NaCl はアルカリと可溶性の酸によって形成される平均的な塩です。 塩化ナトリウムは強電解質です。 イオン間の引力は非常に強いため、極性の高い溶媒のみがそれを破壊できます。 水中では物質は崩壊し、陽イオンと陰イオン (Na + 、Cl -) が放出されます。 それらの存在は、食塩の溶液が持つ導電性によるものです。 この場合の式は、乾物 - NaCl の場合と同じ方法で書かれます。 ナトリウムカチオンに対する定性反応の 1 つは着色です。 黄色バーナーの炎。 実験の結果を得るには、きれいなワイヤーループに少量の固形塩を集め、それを炎の中央部分に追加する必要があります。 食塩の特性は、塩化物イオンに対する定性的反応からなる陰イオンの特異性にも関連しています。 硝酸銀と反応すると、溶液中に塩化銀の白い沈殿物が析出します(写真)。 塩化水素は塩酸より強い酸によって塩から置き換えられます: 2NaCl + H 2 SO 4 = Na 2 SO 4 + 2HCl。 通常の条件下では、塩化ナトリウムは加水分解を受けません。
岩塩の応用分野
塩化ナトリウムは氷の融点を下げるため、冬には道路や歩道に塩と砂を混ぜたものが使用されます。 彼女は吸収する 多数の不純物は溶けると川や小川を汚染します。 道路塩はまた、車体の腐食プロセスを促進し、道路の隣に植えられた木にダメージを与えます。 化学産業では、塩化ナトリウムはさまざまな化学物質の製造原料として使用されます。
- 塩酸;
- ナトリウム金属;
- 塩素ガス;
- 苛性ソーダおよびその他の化合物。
さらに、食塩は石鹸や染料の製造にも使用されます。 キノコ、魚、野菜の缶詰やピクルス用の食品防腐剤として使用されます。 人々の甲状腺機能不全に対処するために、食卓塩の処方は、KIO 3、KI、NaI などの安全なヨウ素化合物を加えることによって強化されています。 このようなサプリメントは甲状腺ホルモンの生成をサポートし、風土病の甲状腺腫を予防します。
人体にとっての塩化ナトリウムの重要性

食卓塩の配合、その組成は非常に重要になっています 重要人間の健康のために。 ナトリウムイオンは神経インパルスの伝達に関与します。 塩素陰イオンは胃内での塩酸の生成に必要です。 でも多すぎる 素晴らしいコンテンツ食品に含まれる食卓塩は高血圧を引き起こし、心臓や血管の病気を発症するリスクを高める可能性があります。 医療では、大量の失血があった場合、患者に生理食塩水を投与します。 これを得るには、9 gの塩化ナトリウムを1リットルの蒸留水に溶解します。 人体は食物からこの物質を継続的に供給する必要があります。 塩分は排泄器官や皮膚から排泄されます。 人間の体内の平均塩化ナトリウム含有量は約 200 g ですが、暑い国では発汗量が多いため、この数値はさらに高くなります。









人の中に神の輝きを見ることは魂にとっての香油である
情報とその人への影響 情報が人に与える影響 - 操作の関係
相続人は亡くなった親族の税金を支払う必要がありますか? 所有者の死後、誰が税金を支払うのでしょうか?
税務当局の事前監査活動の秘密 事前監査分析部門は何をしているのですか?
テーマに関するプレゼンテーション: 東スラブ人の宗教